Slik angriper pest – og slik forsvarer vi oss
Pesten som antakelig sto bak Svartedauden herjar framleis, om enn i langt mindre omfang enn før. No veit vi meir om korleis bakterien angrip oss.
I verda kan fleire tusen menneske bli ramma av pest kvart år. Bakterien Yersinia pestis er årsak til sjukdommen. Denne ga Svartedauden, som rundt midten av 1300-talet tok livet av titals millionar menneske.

“Mor, der kommer en kjærring.” Theodor Kittelsen lagde ein bildeserie over temaet Svartedauden. Pesten var ei gammal kone som dro rundt mellom husa.
Men korleis angriper pestbakterien menneske, og korleis forsvarer kroppen seg mot stadig nye angrep? Ny forsking på bakterien gir nye svar.
«Våpenkapplaup»
Evolusjonen verkar slik at det er sannsynleg at det foregår eit «våpenkapplaup» mellom bakteriar og menneske.
Bakteriane angrip menneskekroppen på nye måtar, men over generasjonar vert menneska betre til å kjempa imot og får større motstandsevne mot desse angrepa. Før bakteriane igjen finn nye metodar for å angripa oss. Sagt på ein annan måte:
– Bakteriane finn måtar å hemma immunresponsar, men kroppen utviklar nye måtar for å omgå blokaden og å kjenna igjen infeksjonen. Vi kan håpa at mennesket vinn til slutt! seier Egil Lien, professor II ved Institutt for kreftforsking og molekylær medisin ved NTNU.
Lien er del av ei gruppe ved forskingssenteret NTNU-Cemir, som mellom anna undersøkjer korleis bakteriar angrip menneske. Dei har denne gongen sett på såkalla «effektorproteiner».
- Les også: Slik dreper svartedaudens bakterie fortsatt
Forvirrar menneskecella
Effektorproteiner er signalstoff frå bakteriar som utløyser ein bestemt reaksjon når dei kjem inn i ei celle. Mange bakteriar som gir sjukdom brukar spesialiserte utskillingssystem for å føra sine effektorproteiner inn i menneskeceller.
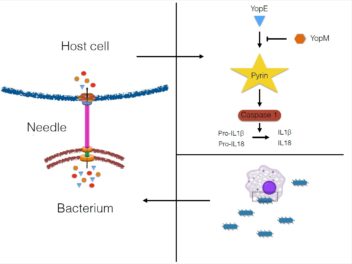
Forskarane har fokusert på korleis bakteriane manipulerer cellenes utskilling av signalmolekyla IL-1b og IL-18. Slik utskilling kan gi anti-bakterielle responsar i pattedyr. Slike signalmolekyl kallast også «cytokiner». Illustrasjon: Pontus Ørning, NTNU-CEMIR
Desse effektorproteinene kan ha forskjellige funksjonar, men hovudmåla er nok å gi eit godt vekstmiljø for bakteriane.
Ved å blokkera immunresponsar i celler kan bakteriane stoppa angrep og bakteriehemmande aktivitetar, noko som ofte er oppgåva til det medfødde immunforsvaret.
Sagt på ein enkel måte – bakteriane kan bruka effektorproteinene til å laga kaos inne i celler, slik at infeksjonen kan spreia seg vidare utan å bli effektivt stoppa.
Fleire metodar
Bakteriane kan overføra effektorproteiner på fleire måtar. Eit av dei best kjende systema er kalla type 3 sekresjonssystem, og finnast i ulike sjukdomsframkallande patogen slik som Salmonella, E. coli, Shigella, Yersinia og andre.
– Desse sekresjonssystema er sofistikerte nanomaskiner. Dei former ei «nål» frå bakterien og lager ei pore i menneskecella som effektorproteinene vert ført inn gjennom, forklarer Lien.
Forskarar tilknytt NTNU-CEMIR har bruka Yersinia pestis – altså bakterien som forårsakar byllepest – som eit modellsystem, eit system som demonstrerer korleis fleire typar bakteriar verkar.
Pesta i trappa
Øinene dybt i dødningskallen,
ruller, rinder,
skjeler og stikker
hvast som syler,
lyser og ser i mørket som katten.
Pesta soper hver en krok.
Slut med raking, sope, sope!
Tiden er knap, alle maa med,
Per og Paal, rub og stub.
Pesta liker sig, veiret er bra,
trist og mørkt.
Limen soper i krik og krok.
Alt er trist, deilig trist.
Død og døde,
stank og raaddenskab.
(Pesta kommer. Th. Kittelsen)
«Svartedauden» var antakeleg ein blanding av byllepest og lungepest, meiner eit fleirtal av dei som har studert feltet.
- Les også: Den lange krigen mot rottene
Bakteriar kontrollerer signalmolekyl
Forskarane ved NTNU-CEMIR har oppdaga korleis nokre av desse bakterielle effektorproteinene kan blokkera nye signalvegar i det medfødde immunforsvaret vårt.
Dei har fokusert på korleis bakteriane manipulerer cellenes utskilling av signalmolekyla IL-1b og IL-18. Slik utskilling kan gi anti-bakterielle responsar i pattedyr. Slike signalmolekyl kallast også «cytokiner».
– Yersinia er svært effektiv i å kontrollera utskilling av disse signalmolekyla. Eit effektormolekyl kalla YopM kan hemma aktivering av eit cellekompleks kalla pyrin-inflammasomer, som regulerer frigjeving av IL-1b og IL-18, seier Lien.
Ein bakteriestamme som manglar YopM og er svekka i normale mus, kan framkalla sjukdomsreaksjonar i mus som manglar pyrin. Slik blei det bevist at denne mekanismen er viktig for immunfunksjonar i pattedyr.
Nye forsvarsmekanismar
Gjennom evolusjon kan menneske utvikle nye forsvarsmekanismar mot slike angrep. Dei som overlever bakterieangrepa vil overføra sine genar og sine evner til å stå imot sjukdomar til neste generasjon.
Over generasjonane kan dei som står imot bakterieangrepa dominera ei heil befolkning, spesielt om ein sjukdom er så skadeleg eller dødeleg at den i stor grad hemmar folks evne til å føre genane sine vidare.
Det kan gje uventa utslag. Som at det kan vera ein fordel å vera utsatt for mindre alvorlege sjukdomar.
- Les også: Attilas arv
Sjeldan sjukdom kan gje større motstand
– Det er interessant at nokre menneske, slik som dei som har den inflammatoriske sjukdomen familiær middelhavsfeber, har mutasjonar i pyrin-molekyla sine. Desse pasientane kan ha auka nivå av IL-1b og IL-18, seier professor Lien.
Ein hypotese er at desse individa kan ha hatt ulik motstand mot infeksjonar, slik som Svartedauden, opp gjennom tidene.
Kan dei ha vore meir motstandsdyktige sidan dei har auka mengder med signalstoffer? Kan dette ha vore ein positiv seleksjonsfaktor, noko som bidrog til at dei i gjennomsnitt fikk fleire barn som overlevde enn dei som ikkje hadde aukt motstand?
Familiær middelhavsfeber er ein sjeldan sjukdom i Noreg. Men den er mykje meir vanleg i for eksempel Tyrkia, som var ein av portalane for innføring av pest frå Asia til Europa under mellom anna Svartedauden.
– Kanskje meir forsking kan finna samanhengar mellom pyrin-mutasjonar, historiske epidemiar og pandemiar, og moderne infeksjonar, seier Lien.
Uansett, CEMIR-prosjekta har så langt funne komplekse interaksjonar mellom bakteriar og vertsorganismar, og vist nye sider av korleis kroppen kjemper mot infeksjonar, påpeiker han.
Referansar:
1. Ratner, D., Ørning, M.P.A., Lien, E. (2016). Bacterial secretion systems and regulation of inflammasome activation. J Leukocyte Biol. Online Nov 3. pii: jlb.4MR0716-330R. http://www.jleukbio.org/content/101/1/165.full
2. Ratner, D., Ørning, M.P.A., Starheim, K.K., Marty-Roix, R., Proulx, M.K., Goguen, J.D., Lien, E. (2016). Manipulation of IL-1b and IL-18 production by Yersinia pestis effectors YopJ and YopM and redundant impact on virulence. J Biol Chem. 291, 9894-905. http://www.jbc.org/content/early/2016/02/16/jbc.M115.697698.abstract
3. Ratner, D., Ørning, M.P.A., Proulx, M.K., Wang, D., Gavrilin, M., Wewers, M., Alnemri, E., Johnson, P., Lee, B., Mecsas, J., Kayagaki, N., Goguen, J.D., and Lien, E. (2016): The Yersinia pestis effector YopM inhibits Pyrin inflammasome activation. PLoS Pathogens 12:e1006035. http://journals.plos.org/plospathogens/article?id=10.1371/journal.ppat.1006035





