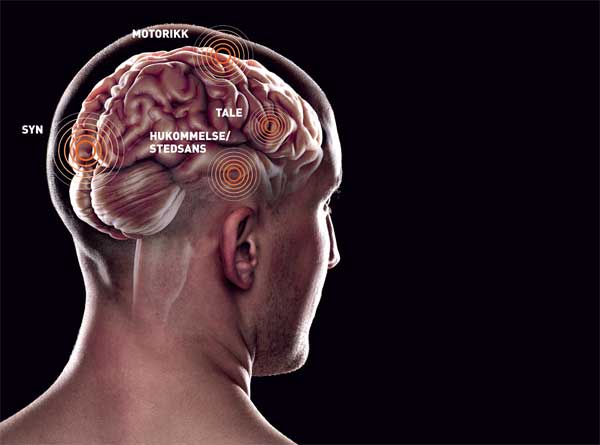
Jakten på hjerneprotesen
Det er ikke nødvendigvis så mange år til du blir nødt til å tenke tanken: Hvis en av dine kjære rammes av sykdom eller skade i hjernen, eller blir født med en hjernesykdom – ville du da byttet ut en del av hennes hjerne, hvis det var mulig? Og ville hun fortsatt være den samme?
Erstatningsdeler til menneskekroppen er en eldgammel del av den medisinske vitenskapen. Både trebein, løshår og juksetenner fantes for tusenvis av år siden.
I vår egen tid forventer vi å få skiftet ut hofteledd, hornhinner og hjerteklaffer når det trengs. Gjenstår det mest kompliserte organet av alle: hjernen.
Hjernesykdommer koster Norge 78 milliarder kroner hvert år, og mer vil det trolig bli når eldrebølgen slår inn for fullt. Arbeidet med å utvikle reservedeler til hjernen er for lengst i gang.

Ny start med hjerneprotese
Ville du gitt din gamle far ny stedsans i bytte mot nerveceller som var rammet av begynnende demens? Når korttidshukommelsen svikter, vil det være galt å sette inn en bunt med nerveceller som kan gi tilbake funksjonen, eller bråstarte læringsevnen?
Foto: photos.com
Reservedeler til hjernen – er det mulig? Og vil vi ha dem?
Mesteparten av sommeren 2011 tilbrakte jeg på et svett stolsete, ved siden av en sykeseng. Der lå et kjært familiemedlem som var overlatt til det beste St. Olavs Hospital kunne by på.
En operasjon gikk ikke helt som forventet, og lenge hang livet og forstanden i en tynn tråd – det vil si i plastrør med blod, medisiner og surstoff.
Da bevisstheten hos pasienten sakte kom tilbake, kom også usikkerheten hos oss pårørende: Ville han bli frisk igjen? Og ville han være den samme gamle?
Når dine nærmeste rammes av sykdom eller skade, vil du ofte søke enhver form for behandling. Ingen stiller spørsmål ved å bruke medisiner som virker inn på hjernen – men hva med en liten transplantasjon?
Ville du gitt din gamle far ny stedsans i bytte mot nerveceller som var rammet av begynnende demenssykdom? Hva med hukommelsen? Når korttidshukommelsen svikter, ville det være noe galt i å sette inn en bunt med nerveceller som kan gi tilbake funksjonen?
Drømmer vi, eller er reservedeler til hjernen nærmere enn vi tror? Er hjernetransplantasjon rett rundt hjørnet?
Med mitt familiemedlem gikk det bra til slutt. Men spørsmålene forsvant ikke. Jeg bestemmer meg for å jakte på reservedeler til hjernen.
Gasspedal og bremsekloss
Jeg har hørt at hjernen har et ekstra beskyttelsesnivå og vil først snakke med en dame som kan si noe om hjernen og immunsystemet. Carla Shatz er professor i nevrobiologi på Stanford University i USA. Hun var den som oppdaget at også nervecellene produserer de molekylene som kroppens immunforsvar bruker for å kjenne igjen fiender.
Jeg har misforstått dette med beskyttelsesnivået, skal det vise seg, og skal få den første av flere overraskelser i jakten på hjerneprotesen.
Shatz og hennes kollegaer har satt seg som mål å finne ut hvordan vår erfaring påvirker utviklingen av nervesystemet. Gjennom studier av synssystemet har de funnet ut at nettopp de genene som brukes i immunforsvaret i kroppen, er selve bryterne som regulerer utviklingen og tilpasningen av sammenkoblingene i hjernen.
– I utgangspunktet har vi trodd at hjernen var såkalt immunprivilegert, forteller Shatz. – Altså at hjernen ikke uttrykker et sånt immunforsvar som kroppen gjør. Sånn sett skulle det faktisk være enklere å transplantere vev inn i hjernen enn resten av kroppen. Men så oppdaget vi at hjernen likevel produserer det som heter MHC klasse 1-molekyler. Forskjellen er at i hjernen brukes de ikke på samme måte som i kroppen.
– Dette genet, MHC, fungerer sånn at hvis du slår det av, så er det som å ta bort en bremsekloss på læringen, forklarer hun. – Og i de dyreforsøkene vi har gjort så langt, blir det vi kaller plastisiteten, hjernens evne til nye koblinger, mye større når vi fjerner MHC-bremseklossen. Det gjelder også hos eldre dyr.
Nye celler, nytt liv
Shatz forklarer at når de har fått komplett oversikt over gasspedalene og bremseklossene i dette systemet i hjernen, så kan man kanskje bråstarte læringsevnen også hos eldre.
– Hva om vi kunne gi en slagpasient en pille som ga hjernen muligheten til å lære på nytt? La de områdene som ikke er rammet av slaget, koble seg om og ta over funksjonene til det slagrammede området? sier hun. – Eller tenk på barn med cerebral parese som har nedsatt læringsevne. Hva om de kunne få regulert opp læringsevnen sin og få et bedre liv? Ville ikke det vært fantastisk, spør hun.
Jeg kan jo ikke være uenig. Alt dette kan skje i framtiden, tror Shatz. For pasienter kan det bli aktuelt å bruke en blanding av spesialiserte stamceller i kombinasjon med medikamenter. Dette kan bedre hjernens koblingsevne for å få de nye nervesystemene til å passe inn med de eksisterende.
Allerede i 1998 ble det gjort forsøk der en parkinsonpasient fikk satt inn nye celler i hjernen. Disse nye cellene skulle erstatte gamle som ikke lenger ville produsere signalstoffet dopamin. Dette ble begynnelsen på nervecelletransplantasjon, og hadde brukbare resultater, men også en del bivirkninger.
Da er det kanskje ikke så enkelt som bare å sette inn friske og arbeidsomme celler?
Drømmen om en bioprinter
I jakten på svar vil tilfeldigheter at jeg kommer i kontakt med den greskfødte hjerneforskeren Ioanna Sandvig. Hun omskolerte seg i sin tid fra økonom til biolog, ved Imperial College i England, etter å ha oppdaget sin kjærlighet til nevrobiologi og til en norsk forsker.
Sandvig har nettopp levert sin doktorgradsavhandling i nevrovitenskap, på NTNU. Jeg møter henne på MR-senteret, den lille røde blokka bak de store nye byggene på St. Olavs Hospital. Hun åpner et perspektiv på reservedeler til hjernen som jeg ikke har hatt fantasi til å tenke på.

Nye nerveceller på vei
Om synsnerven blir skadet, er det ikke bare å stille med erstatningsceller. MI-lab og alginatforskere ved NTNU samarbeider om å utvikle små alginatkuler som fungerer som livmorer. De gir nærende stoffer i et mykt, støttende miljø til nye nerveceller som skal vokse opp. Med ulike MR-bildeteknikker overvåkes vokseprosessen nøye. Til høyre et MR-bilde av en skadet rottessynsnerve (røde piler) med nye nerveceller som følges nøye av forskere (hvit pil).
Nye nerveceller på vei
Om synsnerven blir skadet, er det ikke bare å stille med erstatningsceller. MI-lab og alginatforskere ved NTNU samarbeider om å utvikle små alginatkuler som fungerer som livmorer. De gir nærende stoffer i et mykt, støttende miljø til nye nerveceller som skal vokse opp. Med ulike MR-bildeteknikker overvåkes vokseprosessen nøye. Til høyre et MR-bilde av en skadet rottessynsnerve (røde piler) med nye nerveceller som følges nøye av forskere (hvit pil).
– En gang i framtiden, jeg aner ikke når, men det er jo dette vi jobber fram mot, begynner hun, – da kan jeg se for meg at en pasient kommer inn med for eksempel en akutt hjerneskade, og blir sendt til skanning. Samtidig tar vi en hudprøve eller i hvert fall en eller annen celleprøve. Dette gir oss den genetiske informasjonen som gjør det mulig å designe celler fra grunnen, som matcher pasienten perfekt. Så får vi et tredimensjonalt bilde av skaden fra skanningen. Deretter sender vi denne informasjonen til en bioprinter som kan trykke ut en erstatningsbit til det skadede området.
Jaha, tenker jeg, temmelig satt ut. La gå at det i USA faktisk finnes «skrivere» som kan trykke ut nylaget hud til skadde soldater i krig. Det er det mulig å se for seg. Men er det virkelig sannsynlig at vi kan få skreddersydde hjernebiter?
Sandvig roer meg ned med at det nok vil gå flere tiår før vi kan se snurten av så spesialtilpasset hjelp. Men på veien dit er det både mye å lære og mange gåter å løse.
Alginatlivmor for hjerneceller
Selv har Ioanna Sandvig og dem hun jobber sammen med, fokusert på hvordan man kan få synsnerven til å vokse sammen igjen hvis den blir skadet. Det er vanskeligere enn man skulle tro, å få til reparasjoner inne i hjernen. Nervene skal ikke bare lappes sammen, men er også avhengige av et avansert støttesystem.
Forskeren sammenligner det med en bil som skal krysse en vei som er ødelagt av flom.
– Hvis veien er gått i stykker, hjelper det ikke å fylle bensin på bilen, sier hun. – Det må grunnarbeid til før man kan legge asfalt, og først da kan bilen settes i gang igjen. Sånn er det også med nerver som går i stykker. Både nerven og alt som er rundt, må pleies, i riktig rekkefølge. Det er utrolig komplisert. Det er ikke nok å stille med de rette erstatningscellene.
På Medical Imaging Laboratory (MI-lab) ved NTNU, der hun arbeider, har de et bredt samarbeid med mange andre fagmiljøer. I samarbeid med alginatforskere utvikler de nå små alginatkuler som har et mykt, støttende miljø inne i seg, med massevis av nærende og styrende stoffer for nerveceller eller andre celletyper som skal vokse opp.
– Disse bitte små kulene er som små livmorer for cellene, forteller Sandvig. – Cellene får et oppvekstmiljø som er optimalt. Da øker sjansen veldig for at de overlever når de settes inn i hjernen igjen.
På MI-lab følger de opp de nydyrkede cellene nøye med forskjellige MR-bildeteknikker.
– En type bilder følger utviklingen til cellene vi setter inn. En annen type følger med på om de avrevne nervetrådene begynner å skyte nye skudd og vokse. Så vi kan følge med og overvåke vokseprosessen nøye, forklarer Sandvig.
Jeg lurer på om hun skal lage formstøpte celleklumper snart. Og om hun tror på reservedeler til hjernen. Svaret er kontant:
– Det er nok mange tiår før vi er der. Men vi kommer dit!
Nanopartikler

Arm styres av hjernebølger
Gjennom forskningsprogrammet Human Assisted Neural Devices (Hand) i Darpa er det utviklet en armprotese som er nærmest som en ny biologisk arm. Denne armen styres direkte fra hjernen via opptak av hjernebølger fra sensorer som er plassert direkte på hjernens overflate. Etter hvert håper prosjektet å kunne lage hukommelsesproteser – som for eksempel kan gi minnet tilbake til soldater som skades i kamp.
Om noen tiår, ja. Det er vel omtrent da eldrebølgen slår inn over oss med full tyngde.
I 2050 vil det være nærmere 160 000 mennesker med demens i Norge, hvis statistikerne får rett. Det er godt over dobbelt så mange som i dag. Som skal dele på sykepleiere, sykehjemsplasser og helsekroner.
De fleste som utvikler demens, får Alzheimers sykdom. Den oppdages som regel ved at stedsansen og korttidshukommelsen forverres drastisk. I Trondheim har vi en gruppe hjerneforskere som har jobbet i lengre tid med å kartlegge nettopp disse egenskapene i hjernen, i minste detalj.
May-Britt og Edvard Moser er nestleder og leder ved Kavli Institute for Systems Neuroscience på NTNU. Deres forskning har vist hvordan nervecellene i et bestemt område i hjernen både lagrer minner, gjør lignende minner ulike, hvordan vi henter dem fram igjen, og hvordan det hele kobles sammen med stedsansen – som de også har avslørt grunnprinsippene for.
Men hva tror de om mulighetene for å erstatte ødelagte deler av hjernen med nye?
– Transplantasjon har jo lenge blitt utført i form av såkalte grafts, forteller Edvard Moser.
– Man setter for eksempel inn stamceller i hjernen hos pasienter med Parkinsons sykdom. Så det å korrigere for sviktende funksjon gjør vi allerede.
Vi ser stadig oftere eksempler på at elektroniske proteser samarbeider med nervesystemet, eksempelvis sneglehusimplantat i øret og mekaniske hender. Kanskje man etter hvert kan fylle hjernen med funksjonell elektronikk?
– Vi kan nok få hjernevev til å interagere med elektroniske kretser, sier Moser. – Men jeg ser ikke helt for meg grensesnittet ennå. Generelt kan vi si at jo mer spesifikke oppgaver og jo færre celler og funksjoner som er involvert, desto mer realistisk er tanken.
Moser har ingen tro på at det vil fungere å transplantere større deler av en hjerne.
– Det skal mye til for at det man tilfører, kobles opp med resten av hjernen på den rette måten, i alle fall med det vi vet i dag. Men jeg tror nok at man en gang kan transplantere inn celler eller nanopartikler som utfører spesifikke oppgaver rundt om i hjernen, avslutter han.
Dingser som bygger bro

Elektronikken gir ham språk
Steven Hawking lider av en sjelden variant av amyotrofisk lateralsklerose (ALS). Lidelsen lenker ham til rullestolen og gjør det umulig å kommunisere direkte med omverdenen. Han arbeider med en spesiallaget språkcomputer som blir styrt av hans øyne og enkelte muskler i ansiktet.
Foto: wikipedia
De som derimot har tro på dette, er det amerikanske forsvarets senter for avansert forskning, Darpa (Defense Advanced Research Projects Agency).
Gjennom forskningsprogrammet Human Assisted Neural Devices (Hand) i Darpa er det utviklet en armprotese som er nærmest som en ny biologisk arm. Denne armen styres direkte fra hjernen via opptak av hjernebølger fra sensorer som er plassert direkte på hjernens overflate.
Hand-prosjektet går nå videre med detaljert kartlegging av hvordan korttidshukommelsen virker. Formålet er å gi tilbake hukommelse til dem som skades i kamp, ved å skape «dingser» som bygger bro over de skadede delene i hjernen.
Det er jo lov å håpe at teknologien vil gi oss soldater med hukommelsesproteser, også kan gi sivile som sliter med hukommelsen, hjelp på sikt.
Et etisk problem?
Så langt er det flere utfordringer enn løsninger. Men ingen er uenig i hvilken vei det går: Vi vil få reservedeler til hjernen, i en eller annen form og størrelse.
Men hva gjør vi den dagen vi står der med en ødelagt stedsans – og med en flunkende ny erstatningsbit i hånden? Er det bare å sette den inn? Eller har vi skaffet oss et etisk problem?
Leif Edward Ottesen Kennair er førsteamanuensis på Psykologisk institutt ved NTNU. Han er evolusjonspsykolog, og opptatt av menneskets natur. Jeg spør om han ville anbefalt å bruke reservedeler i hjernen.
Han svarer med et kontant ja: – Vi gjør det allerede med tanke på hørsel. Og hvem vil moralisere over bruk av krykker? Dersom det er en ekte reservedel, så erstatter det en tapt funksjon. Jeg tror at da bør man fra et legeetisk perspektiv si ja.
Bruk av reservedeler er reiser ikke de store etiske spørsmålene for psykologen.
– Jeg ser for meg at man kunne lage mekanismer som erstatter tapte mekanismer, sier han.
– Dersom man kan få til muligheten for nervevekst, trenger man kanskje ikke kartlegge hjernen så detaljert mekanisk. Kanskje det holder å få til cellevekst av celler som har en bestemt funksjon. For meg handler ikke dette om å ‘tukle’ med hjernen eller personer; det handler om å erstatte mistede evner med tilsvarende evner.
Kennair er likevel ikke overbevist om at vi vil få reservedeler med det første.
– Det er så mye man må avklare før man konkluderer, sier han. – Å lage en anatomisk modell av hjernen slik den er fysisk, altså slik den er med nerveceller som er koblet sammen og kommuniserer, det er én sak. Spørsmålet er om forskere også klarer å bygge en kunstig hjerne som også fungerer funksjonelt. Ellers sitter man jo igjen med et kjempeavansert romskip som man ikke aner hvordan man skal fly.
– Man klarer helt sikkert å beskrive hvordan hjernen er. Men vi psykologer jobber jo fortsatt med å besvare spørsmålet «Hva er det den gjør?»
– Sjelen finnes ikke
La oss likevel tenke oss at våre kjæres hjerner gradvis forfriskes med nytt nervevev. Hva skjer den dagen mamma tilsynelatende er i super form etter en hjerneoperasjon, men har glemt oss barna? Er hun da dement, eller er hun frisk og med ny bevissthet?
– Nytt nervevev er ikke en protese, det er en tilhelet kroppsdel, sier Kennair. – Det er organisk, ikke mekanisk. Jeg tenker da at mamma vil oppleve og lære ting på nytt, og bli vurdert på lik linje som andre med hukommelsestap. Graden kan være mild til alvorlig, men nå har hun en mulighet til å lære og å huske på nytt igjen.
Hva med sjelen, vil vi vite.
– Sjelen finnes ikke, slår Kennair fast. – Identitet eksisterer, og den er en funksjon av nevral aktivitet. Det ser man i mange nevrodegenerative lidelser. Sånn sett burde man få tilbake identitet dersom avgrensede funksjoner som er tapt, erstattes med faktisk fungerende kretser.
Ressurs og rettferdighet
Filosof Allen Alvarez på NTNU forsker på etikken rundt menneskelig forbedring. Han mener det er for snevert bare å se på hvert enkelt menneske og deres eventuelle forbedring ved en hjernetransplantasjon. Det handler etter hans mening både om ressurser og om identitet.
– Det brukes jo enorme summer penger for å forske fram og utvikle det som skal til for å kunne lykkes med å dyrke nervevev eller foreta transplantasjoner, sier Alvarez. – Det blir da et spørsmål om fordeling og rettferdighet, særlig hvis dette er penger som ellers ville blitt brukt på behandlinger som allerede har en kjent og god effekt.
– Finnes det for eksempel en prinsipiell måte for å avgjøre hvorvidt vi bør investere store summer i å utvikle framtidig medisinsk teknologi, framfor å bruke pengene på utvidet helse og omsorgstilbud i eget eller andre fattige land, spekulerer filosofen.
Alvarez mener at det er flere faktorer som påvirker om det er moralsk riktig å investere i utvikling av teknologier som hjernetransplantasjon. – Både størrelsen på behovet, og hva det vil koste oss som samfunn, spiller inn, sier han.
Filosofen lanserer så et helt annet problem som ikke handler om ressursfordeling, men om deg som menneske, og din identitet: hvem du er.
Bare biologi?
– Når det gjelder bevisstheten, vet vi jo ikke nok om den til å kunne avgjøre om det er noe som kan flyttes med en hjerne eller ikke, sier han. – Dette er kontroversielt uansett hvilket fagfelt du ser det fra, og er langt fra forstått. Er hjernen alene grunnlaget for bevisstheten, eller handler det om samhandling mellom hjernen og kroppen?
Filosofen lanserer et tankeeksperiment.
– Hva om vi kunne transplantere bevisstheten alene, begynner han. – Kanskje laste den opp i en datamaskin? Hva er det egentlig som utgjør deg selv, din identitet? Er det hjernen alene? Hjerne og kropp? Må hjerne og kropp leve og forholde seg til omgivelser for å eksistere?
Man kan få hodepine av å tenke på slikt. Og Alvarez har flere etiske problemstillinger på lager:
– Hva med beslutningene, spør han. – Hvem skal bestemme om en person skal gjennomgå en hjerneoperasjon med transplantasjon dersom denne personen ikke er i stand til å fatte beslutninger for seg selv? Hva sier vi den dagen noen ønsker å gjennomføre en prestasjonsfremmende transplantasjon? Hva med å slippe å gjennomgå transplantasjon, dersom dette viser seg å bli den vanlige eller rimeligste behandlingsmetoden – skal man kunne nekte?
Etterhvert som vi får mer kunnskap om hjernen, mener filosofen, vil våre etiske dilemmaer endre seg i takt med endringer i oppfatningen av oss selv som bevisste mennesker.
– Et helt annet dilemma, sier Alvarez, – er hvis forskningen ender opp med å si at de beslutningene vi tar, ikke baserer seg på fri vilje, men tvert imot er et resultat av elektriske signaler i hjernen utenfor viljemessig kontroll. Da ville vi sitte igjen uten moralske dilemmaer fordi våre handlinger ville være avhengig av nervesignaler og ikke vilje. Dilemmaene ville simpelthen slutte å være dilemmaer.
Alvarez er nå i gang med et prosjekt der han og kollegaer fra University of British Columbia undersøker hva folk tenker omkring det å gjennomføre prestasjonsfremmende, eller kroppsforbedrende, tiltak. Neste år får vi vite hvordan den yngre generasjon stiller seg til dilemmaer omkring livsforlengende medisin; hvorvidt de aksepterer radikale syntetiske midler, nanoteknologiske implantater, eller bare naturlige; hvilke tanker de gjør seg om befolkningsvekst dersom vi alle skulle bli vesentlig eldre; og en rekke andre problemstillinger som vi sannsynligvis vil møte i løpet av de kommende tiår.
– Et luksusproblem
Jeg blir stadig mer i villrede. Hvordan skal vi fatte kloke beslutninger? Og hva bør vi prioritere?
Helse er også politikk, og jeg kontakter statssekretær Robin Kåss i Helse- og omsorgsdepartementet. Med bakgrunn som allmennlege har han møtt sin andel av de eldre som opplever at hjernen begynner å svikte.
– Vi er oppmerksomme på at hjernesykdommer er et økende problem ikke minst som følge av en aldrende befolkning, sier han. – Derfor har vi allerede i Nevroplan 2015 hatt skarpere fokus på dette, og deltar i tillegg aktivt i etableringen av et fellesprogram for demensforskning i EU.
– Hovedproblemet i dag er at det ikke finnes noen særlig grad av kurativ behandling, altså behandling som gjør deg frisk og ikke bare lindrer litt av symptomene, sier han. – Vi har jo gjort veldig store framskritt i kampen mot hjerte- og karlidelser, og kreft. Men vi har ikke hatt den samme framdriften når det gjelder hjernesykdommene.
Kåss synes det er utfordrende at vi fordi vi lever lenger, blir vi stadig flere med demenssykdommer. Jeg spør hva han tror vil skje den dagen muligheten byr seg til å bytte ut alzheimersyke hjerneceller med friske biter hjernevev. Vil det være løsningen som kan gi eldre mennesker flere gode år, og færre av dem i sykehjemskø?
– Når det er så mange som lider, er den viktigste utfordringen å finne ny kunnskap, å få en større forståelse for hjernen, sier Kåss. – Det er ikke tvil om at nye behandlingsformer vil utfordre oss og reise etiske spørsmål. Det kan bli behov for en grundig debatt, og stortinget skal få siste ord i den saken. Vi får ta det som et luksusproblem den dagen en slik behandling kommer.
Legemiddelindustrien
Mye å spare
Hjernesykdommer koster Norge 78 milliarder kroner hvert år, viser en ny europeisk rapport om kostnader ved hjernesykdommer i Europa. Dette omfatter også de indirekte kostnadene som er beregnet å utgjøre totalt 40 prosent av de 78 milliardene – fravær fra arbeid, svekket funksjonsevne og liknende forhold.
Foto: Geir Mogen
Så spørs det om pengene vil være det som hindrer nye behandlingsmetoder for hjernesykdommene. En ny europeisk rapport om kostandene ved hjernesykdommer peker på to bekymringsfulle utviklingstrender: Legemiddelindustrien flytter ut av Europa til USA, Kina og India fordi Europa ikke klarer å enes om patent og godkjennelsesordninger for legemidler. Samtidig er industrien skuffet over avkastningen på investeringene i forsking på hjernesykdommer, ifølge rapporten. Det har også vist seg vanskeligere å oppnå gode forskningsresultater for disse sykdommene, og det er generelt vanskeligere å oppnå godkjenning for behandling som skal påvirke sentralnervesystemet. Dette medfører at flere legemiddelbedrifter avslutter sine engasjement innenfor hjerneforskning.
Administrerende direktør Karita Bekkemellem i Legemiddelindustrien (LMI) mener at det på ingen måte er legemiddelindustrien som stopper utviklingen av nye legemidler som kan erstatte etablerte behandlinger.
– Legemiddelindustrien arbeider fortløpende med nye legemidler for sykdommer det allerede finnes behandling for, ikke minst fordi både myndigheter og pasienter krever stadig bedre og sikrere legemidler. Dermed vil det alltid være en konkurranse for etablerte behandlingsmetoder, sier hun.
– Her fungerer vanlige markedsmekanismer hvor et legemiddelselskap utvikler et legemiddel som vil konkurrere med produkter fra et annet selskap. Samtidig vil selskapene videreutvikle og gjøre sine egne legemidler bedre og mer kostnadseffektive for fortsatt å være den foretrukne behandlingen, sier Bekkemellem.
Hun kaster ballen videre til myndighetene.
– Ut fra ambisjonene om at forskningen skal utgjøre tre prosent av bruttonasjonalproduktet, kan jo ikke myndighetene være særlig fornøyd selv heller. En større satsing på framtidsrettet bioteknologi kan gi en betydelig økning av forskning i norsk næringsliv, samtidig som det legger til rette for flere medisinske framskritt, ser Karita Bekkemellem.
Frankensteins monster?
Jeg har snakket med mange kloke mennesker. Men jeg vet fortsatt ikke om vi – hvis og når den tid kommer – skal gripe mulighetene og ikke se oss tilbake. Eller om vi faktisk bør tenke oss om noen ganger. For litt nifst er det unektelig, å tukle for mye med det fineste organet vi har. Enn om vi mister kontrollen? Enn om vi av vanvare skaper et monster, slik vitenskapsmannen Vitor Frankenstein gjør i Mary Shelleys roman fra 1818, der han syr sammen et nytt vesen av kroppsdeler fra døde mennesker?
Det kan virke som om frykten for nettopp å miste kontrollen over et menneskes personlighet, og ende opp med noe som er verre enn utgangspunktet, er kjernen i motstanden mot å tukle med hjernen.
Dette har ikke stanset de kunnskapssøkende forskerne. Går vi knapt femti år tilbake i tid, finner vi et kappløp mellom USA og Russland som handlet om å lede an i vitenskapen. I mer eller mindre groteske filmsnutter som ligger åpent ute på nettet, kan vi se hvordan både amerikanske og russiske forskere dokumenterte sine eksperimenter med hodetransplantasjoner, eller fullkroppstransplantasjoner som det gjerne kalles.
I Russland på 1950-tallet utførte Vladimir Petrovich Demikhov forsøk på hunder. Han koblet hundehodet fra kroppen og lot det leve videre, bare koblet til en blodpumpe. Senere transplanterte han et valpehode på nakken til en voksen hund. I en av filmene fra hans laboratorium kan du se hvordan det transplanterte valpehodet og den voksne hunden drikker fra hver sin skål, samtidig.
Menneskehjerter, apehoder
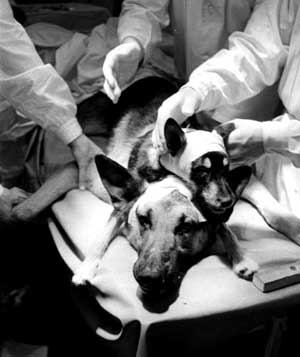
Nytt hode – ikke nytt
I Russland på 1950-tallet utførte Vladimir Petrovich Demikhov forsøk på hunder. Han koblet hundehodet fra kroppen og lot det leve videre, bare koblet til en blodpumpe. Senere transplanterte han et valpehode på nakken til en voksen hund. I en av filmene fra hans laboratorium kan vi se hvordan det transplanterte valpehodet og den voksne hunden drikker fra hver sin skål, samtidig.
Foto: Wikipedia
Den sørafrikanske kirurgen Christiaan Barnard så Demikhov som sin lærer og inspirator. Han besøkte også Demikhovs laboratorier to ganger.I 1967 ga Barnard et nytt hjerte i tidlig julegave til den 54 år gamle grønnsakshandleren Louis Washkansky. Washansky døde 18 dager senere av lungebetennelse, men dette var den første vellykkede hjertetransplantasjonen på et menneske. I dag gjennomføres det på verdensbasis omtrent ti hjertetransplantasjoner hver eneste dag. Den som har overlevd lengst med nytt hjerte, hadde det i over tretti år.
Også Dr. Robert Joseph White, USAs pionér på transplantasjonsfronten, besøkte Demikhovs laboratorier. White er sannsynligvis også den første amerikaneren som har undersøkt Lenins hjerne.
Inspirert av Demikhovs arbeid, flyttet White hode og hjerne fra en apekatt til en annen apekatts kropp. En dags arbeid for flere kirurger tok det å koble sammen blodsystem mellom hode og ny kropp. I et intervju forteller den nå avdøde Dr. White hvordan han opplevde minuttene etter operasjonen:
– Vi så elektrisk aktivitet på registreringene i hjernen. Det var som å gå gjennom en låvedans, alle var ekstatiske. Etter hvert kunne vi se at anestesien begynte å gi seg. Vi så at øyelokkene begynte å bevege seg og at leppene begynte å bevege seg. Dyret var våknet. Det var ikke et lykkelig dyr, det kunne jeg se. Vi tok viskelærsiden på en blyant og rørte ved tennene til apekatten, da bet den etter blyanten. Vi ringte med en bjelle, en lyd den ikke liker. Vi så reaksjonen. Den kvelden innså jeg at vi hadde gjennomført noe monumentalt, enten bra eller dårlig. Jeg innså at det vi hadde gjort for apen, kunne vi også gjøre for mennesker, sa Dr. White.
Dette var i 1970. Apekatten levde videre noen dager og var, så langt Dr. White forteller, bevisst i like stor grad som før operasjonen. Men den var lam fra halsen og ned, fordi ryggmargen var kuttet av.
White var medisinsk konsulent på filmen «The X-Files: I Want to Believe», og grunnla pave John Paul den andres komité for bioetikk. Han var en slags nevrokirurgiens eldregeneral og hadde som motto å arbeide for retten til liv i alle aldre.
Nevrale proteser
Ut over på 1970-tallet ble det eksperimentert med mange typer nevrale proteser. I 1978 kom William Dobelle med det første kunstige øyet. Riktignok var det bare snakk om 68 elektroder som ble koblet direkte inn i synsbarken i hjernen til en mann, «Jerry», som ble blind som voksen. Og «Jerry» fikk ikke synet tilbake, men opplevelsen av å se lysflekker var der.
I 1998 lyktes forskere med å koble sammen hjernen og elektroder på en slik måte at pasienten etter hvert kunne styre datamaskinens musmarkør med hjernen alene. Pasienten, Johnny Ray, var «låst inne» i sin egen kropp uten mulighet for å røre seg, etter å ha fått et slag i hjernestammen. Samme år ble det for første gang satt inn spesialiserte nerveceller som produserer signalstoffet dopamin inn i hjernen til en parkinsonpasient, for å erstatte ødelagte celler av dette slaget.
De siste ti årene har det dukket opp en rekke varianter av proteser. Gode koblinger mellom nerveceller og elektronikk har blant annet gitt mennesker funksjonelle kunstige hender. Den siste utgaven av en slik hånd styres med tankens kraft.

Skredderprinting av hjerneprotese
Allerede nå kan man printe hud – lag for lag – direkte på et sår. I framtiden håper man å kunne printe ut den kroppsdelen eller hjernedelen man trenger.
Foto: Gismag
Nå i høst ble det for første gang godkjent forsøk med å sette inn stamceller for å helbrede ødelagte ryggnerver hos mennesker. Behandlingen har vært lovende hos dyr, men det er nok lenge til ryggskadde kan slippe rullestolen med stamceller.
Menneske – maskin
Et godt eksempel på samarbeid mellom menneske og datamaskin er den kjente britiske matematikeren og astrofysikeren Steven Hawking. Hawking lider av en variant av amyotrofisk lateralsklerose (ALS) som lenker ham til rullestolen og gjør det umulig å kommunisere direkte med omverdenen. Hawking arbeider med en spesiallaget språkcomputer som blir styrt av øynene og enkelte muskler i ansiktet. Elektronikken gir ham et språk.
Samspillet mellom hjerne og elektronikk finner vi ikke minst i spillverdenen. I et spilt som Mindflex er det spillerens hjernebølger som påvirker en balls ferd gjennom en hinderløype.
Syntetisk hjerne
Det første store prosjektet som så for seg å skape en komplett syntetisk hjerne, var det europeiske Blue Brain-prosjektet, som begynte i 2005. Tre år senere hadde forskerne bygd ferdig den første hjernebiten med 10 000 celler. I juli 2011 hadde de økte dette til en nervekrets med en million celler.
Blue Brain har nå gått over i en ny fase. I videreføringen Human Brain Project, et stort europeisk samarbeidsprosjekt med 13 forskningspartnere fra ni europeiske land, er målet å ha bygget en komplett modell av den menneskelige hjerne i år 2023. Med hundre milliarder nerveceller.
Og her ender min jakt på den kunstige hjernen. Uansett hva vi måtte mene om saken: Alt tyder på at vi for lengst er inne i en æra der hjernen ikke lenger er den siste uinntagelige jungelen. Den begynner tvert imot å bli både kartlagt og forstått.
Hjernehjelpen er snart underveis.