Klimavennlig metallproduksjon – hvorfor er det vanskelig?
De fleste vet at metaller lages fra malm, men hvordan lager man egentlig “gull av gråstein”? Det er akkurat den prosessen vi må forstå for å kunne gjøre metallindustrien klimavennlig. Her er alternativene for CO2-fri metallproduksjon.
Skal vi komme i mål med det grønne skiftet, også globalt, trenger verden nye materialer, og ikke minst metaller. I dag er karbon særdeles populært i metallindustrien og årsaken er at det har evnen til å fjerne oksygen fra malmen slik at vi får tak i metallet. I den prosessen dannes CO2, drivhusgassen som vi må unngå i framtiden. Nå skal vi ta fatt på oppgaven å finne andre måter å utvinne metaller på, men hvilke alternativer har vi egentlig?
For å sikre en framtid med utbygging av sol- og vind-energi, værsikre veier og byer over hele verden må vi kunne lage metaller på en sikker, klimanøytral og ansvarlig måte. Vi må selvfølgelig bli bedre på å ta vare på og gjenbruke eller resirkulere det som finnes av metallholdig avfall, men det vil ikke være nok. Skal vi komme i mål med det grønne skiftet, også globalt, trenger verden nye materialer, og ikke minst metaller. I dag slipper metallindustrien ut drivhusgasser og i Norge står den for 10 prosent av det totale CO2-uslippet. Det er derfor presserende å finne nye muligheter for mer klimavennlige alternativer til dagens prosesser.
Tre nøkler til framtidens metallproduksjon
Figuren (lenger ned i saken) viser hvilke stoffer som har evnen til å fjerne oksygen fra malmer, disse kalles reduksjonsmiddel. I det nedre, venstre hjørnet ser vi karbon som i dag brukes til å omvandle nesten alle typer av malm til metall. Historisk har karbonet vært trekull eller tre, men i moderne tid er det stort sett fossilt karbon som brukes. Organiske stoffer slik som trevirke og andre former av biokarbon er ikke rene former av karbon, disse finner vi på linjen mellom karbon og hydrogen. Her finner vi også utradisjonelle biologiske karbonkilder som biogass. Mange metallprodusenter ser på disse reduksjonsmidlene som de mest interessante fordi man forventer å kunne tilpasse dem til dagens produksjonsmetoder, istedenfor å utvikle helt nye prosesser. Imidlertid vil bruk av alle karbonholdige reduksjonsmidler føre til dannelse av CO2. For å unngå at dette fører til en økning i drivhuseffekten må man da enten bruke CO2-nøytrale karbonkilder (f.eks biokarbon) eller fange og lagre CO2 fra avgassen. Klarer man å gjøre begge samtidig kan vi få CO2-negative prosesser i fremtiden, noe flere mener vil være nødvendig for å nå klimamålene. De såkalte karbonnøytrale løsningene har imidlertid også en forsinkelse, da det tar i snitt 90 år før et nytt tre har vokst opp og forbrukt den CO2-mengden som er sluppet ut, og det er for seint om man skal nå Parisavtalens mål.
Trenger enorme mengder karbon
Det store spørsmålet rundt karbon, er hvordan tilgangen på biokarbon vil bli i fremtiden. I tillegg må vi må også tenke på innvirkningene på det biologiske mangfold og andre viktige miljøaspekter. Det er, dessverre, enorme mengder karbon som trengs innenfor metallsektoren. I et langtidsperspektiv er det heller ikke sikkert at karbon er det beste alternativet vi kan finne.
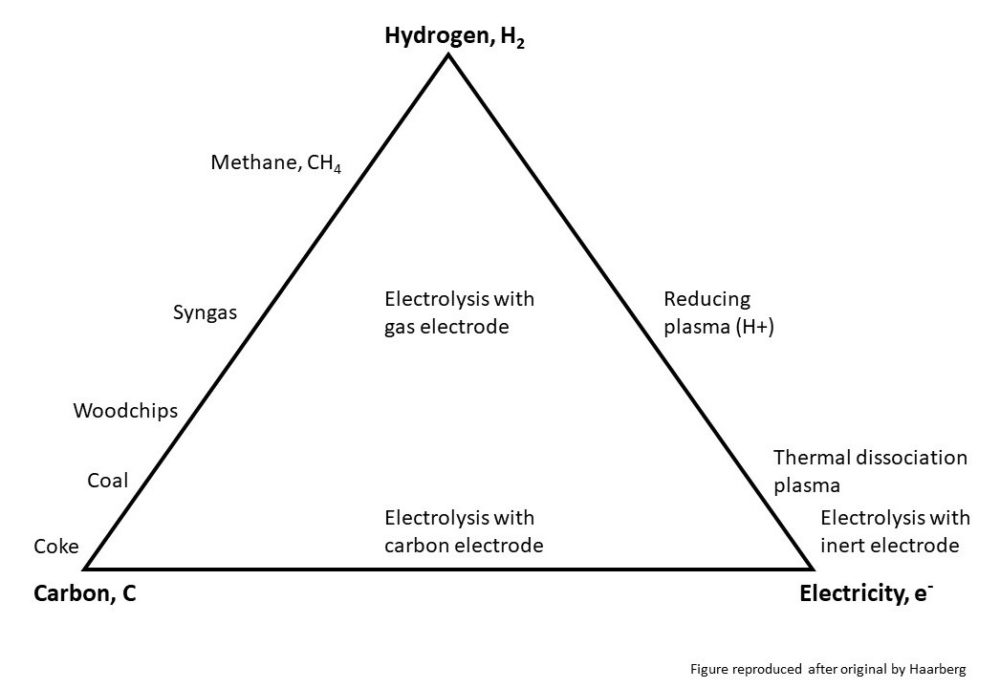
Figuren ( under) viser et mulighetskart over hvilke stoffer som har evnen til å fjerne oksygen fra malmer, de som kalles reduksjonsmiddel.
Kan energi erstatte reduksjonsmidler?
I figurens nedre, høyre hjørne, har vi elektrisitet. Mange vet at for eksempel aluminium lages ved elektrolyse og da bruker man i hovedsak elektrisitet for å få oksygenet i malmen å slippe taket på metallet. Dagens elektrolyseteknologi ligger imidlertid et stykke mot karbonhjørnet i figuren, da man trenger elektroder laget av karbon i elektrolysen. Karbonelektrodene forbrukes i prosessen slik at man egentlig kombinerer effektene av elektrisitet og karbon. Hvis man i fremtiden kan bruke andre typer elektroder, og aller helst typer som ikke blir brukt opp i prosessen, så kunne man i teorien laget metall med kun elektrisitet som erstatter reduksjonsmidlene. I dag brukes store ressurser rundt omkring i verden på å finne opp nye elektrode-løsninger for forskjellige elektrolyseprosesser for forskjellige metaller. Energioptimister ser for seg en framtid med store mengder tilgjengelig fornybar energi, og hvis disse prognosene slår til vil slike energiintensive prosesser bli enda mere attraktive både fra et økonomisk perspektiv og et miljø-perspektiv.
Hvis vi ser litt nærmere på elektron-hjørnet, ser vi at det faktisk finnes enda en mulighet der, nemlig plasma. Hvis man kan bruke tilnærmet ubegrensede mengder energi, kunne det faktisk vært mulig å lage metall uten annet reduksjonsmiddel enn ren energi. Men da er det ekstremt mye energi som skal til, og dette vil nok bare være mulig i de aller mest optimistiske energiscenariene.
Høyinteressant hydrogen
I figurens øvre hjørne har vi hydrogen som er særdeles interessant av mange grunner, ikke minst fordi hydrogen finnes i overskudd i dag siden hydrogen dannes som et biprodukt fra flere forskjellige industriprosesser. Per i dag har vi dessverre ikke mulighet å ta i bruk alt hydrogen vi har tilgjengelig, først og fremst på grunn av utfordringer rundt transport, lagring og sikkerhet. Man kan også lage hydrogen fra naturgass, biogass eller vann (via elektrolyse), . Imidlertid har ikke hydrogen evnen til å omvandle alle typer malmer til metall, men det finnes kanskje muligheter å kombinere hydrogen med andre reduksjonsmiddel for å gjøre det mer potent?
Hydrogen kan samarbeide
På triangelens høyre sidelinje finnes enda et høyenergetisk alternativ, nemlig hydrogen-plasma, hvor det er tilført så mye energi at hydrogenatomene har gått i oppløsning. Hydrogen-plasma er mye mer potent som reduksjonsmiddel enn vanlig hydrogen-gass og kan brukes på mange flere malmer. Da trengs mer energi enn for gass-reaksjoner men betraktelig mindre enn om man skal lage plasma av selve malmen. En annen framtidig mulighet dreier seg om gass-elektroder for elektrolyseprosesser. Her kan man se for seg at hydrogen-gass brukes som reduksjonsmiddel i en elektrolyse-celle.
En annen sterk kandidat for slike gass-elektroder er metan-gass. En gass som i dag lettest fås fra naturgass, men som i fremtiden vil kunne komme fra biologiske kilder, det vil si biogass. Metan kan enten være en måte å tilsette hydrogen til en prosess, eller det kan være et reduksjonsmiddel i seg selv. Kombinasjonen mellom hydrogen og karbon i metan gjør dette til et meget interessant alternativ for metallfremstilling i fremtiden.
Andre gasser som kan brukes for å tilsette hydrogen til prosesser er ammoniakk, som i likhet med metan er mindre eksplosiv enn rent hydrogen og derfor lettere å transportere og lagre. Men bare det å bruke gass som reduksjonsmiddel stiller store krav til omstilling i metallindustriene hvor man vil måtte utvikle og investere i nye typer av reaktorer.
Kan metaller lage metaller?
Vi bør også nevne at mange metaller kan være reduksjonsmiddel for andre metaller, selv om det ikke er tatt inn i figuren her. For eksempel kan aluminium være reduksjonsmiddel for mange andre metaller og også silisium som f.eks. trengs i solceller og elektronikk. Problemet med det er jo at man først må produsere aluminium, noe som i dag ikke skjer uten CO2-utslipp. Så en slik type metallfremstilling vil være helt avhengig av at vi får på plass metoder for å både lage og resirkulere de nye reduksjonsmidlene på en klimanøytral måte.
Hvorfor ikke resirkulere karbonet?
Når vi snakker om resirkulering, er resirkulering av karbon en slags hellig gral. Det ville vært et ekstremt interessant alternativ, da karbon kan produseres uten fossile råmaterialer og samtidig ville resirkuleringen være med på å minke trykket på biologiske karbonkilder, som skogen. Hvis man kunne ha fanget CO2 fra avgassen og deretter splittet det opp til oksygengass, som kan slippes ut, og en karbon-form som kan puttes tilbake inn i ovner og/eller elektrolyseseller, hadde det vært en meget attraktiv løsning.
Utfordringen er at CO2 er så utrolig stabilt at det vil trenges vanvittige mengder energi for å splitte den. Energimengden kan muligens reduseres noe ved å bruke høyteknologiske katalysatorer, som for eksempel Cerium-holdige partikler eller biologiske organismer som alger eller bakterier.
Det finnes altså mange forskjellige alternativer som alle har både fordeler og ulemper. Det er imidlertid god grunn til å tro at noen av disse alternativene kan være nøkkelen til å realisere fremtidens klimanøytrale metallindustri.
Fakta om de ulike stoffene som kan brukes i metallproduksjon:
Hydrogen:
Hydrogen er i seg selv karbonfritt, men kan produseres på mange forskjellige måter der ikke alle er like miljøvennlige. Man opererer derfor med flere ulike begrep, som sier noe om hvordan hydrogenet er produsert.
Grått hydrogen: Hydrogen produsert fra naturgass, med utslipp av 8 tonn CO2 per tonn hydrogen. Det meste av hydrogen i bruk i dag produseres på denne måten.
Blått hydrogen: Hydrogen produsert fra naturgass med fangst og lagring av CO2. Noe CO2 slippes ut under produksjon av naturgass, og fangst og lagring er ikke 100 prosent effektivt.
Grønt hydrogen: Hydrogen som er produsert nært 100 prosent uten CO2-utslipp. Den vanligste måten er ved å bruke fornybar elektrisitet til å spalte vann i hydrogen og oksygen.
(Turkis hydrogen: Hydrogen produsert fra naturgass der karbondelen ikke konverteres til CO2, men i stedet tas vare på som et eget produkt, såkalt "carbon black". Dette kan brukes i f.eks. bildekk.)
Plasma:
Plasma er, sammen med fast stoff, flytende stoff, og gass, en av fire tilstander et stoff kan opptre i.
På samme måte som en væske vil koke og gå over til gass når den varmes opp, vil en gass igjen gå over til plasmaform når den varmes opp nok. Vann koker ved 100 °C, men vanndamp går ikke over til plasmaform før ved nærmere 12000 °C ! Imidlertid kan man senke overgangstemperaturen ved hjelp av elektrisk strøm (Det er dette som gjøres i lysrør. Man sender strøm gjennom en gass og lager plasma, og når plasmaen går tilbake til gassform avgir den lys). I plasmaform splittes et stoff i sine mindre byggeklosser. F.eks. vil vann (H2O) skilles til hydrogen- og oksygenkomponenter. Atomene i en plasma er veldig reaktive og vil kunne reagere med stoffer der man ikke ville fått reaksjon i andre tilstander. For metallproduksjon er dette relevant ved at et plasma kan reagere med oksygenet i en malm og etterlate rent metall. Man kan også tenke seg å lage plasma av en malm, og slik skille oksygen og metallatomene, men dette vil kreve veldig mye energi.
Biokarbon:
Mesteparten av karbonet som benyttes industrielt i dag er av fossilt opphav, f.eks. steinkull, olje, naturgass. All CO2 som slippes ut fra slikt karbon i en industriell prosess kommer i tillegg til det naturlige karbonkretsløpet og bidrar til den økningen av CO2-konsentrasjon vi har sett i siden førindustriell tid.
Med biokarbon menes karbon av biologisk opphav, f.eks. fra trær eller jordbruksavfall. Dersom man ikke høster mer biokarbon enn det som naturlig gror, vil slikt karbon være en del av det naturlige karbonkretsløpet og ikke føre til en endring i CO2 i atmosfæren over tid. Noen peker imidlertid på at det kan ta opptil 90 år for et tre å gro til full størrelse og at det da blir feil å se på biokarbon som en løsning på karbonnøytralitet innen 2050.
Noen nøkkelord:
- Biokarbon: Til tross for at navnet kan synes å indikere alt karbon av biologisk opphav, brukes biokarbon som regel i betydningen "biokull", dvs. trekull.
- Bioolje: Flytende biprodukt fra produksjon av trekull. Inneholder mange av de samme komponentene som fossil olje.
- Biogass: Gass med lignende sammensetning som naturgass (metan og karbondioksid) som dannes ved forråtnelsesprosesser av biologisk avfall.
Elektrolyse:
Elektrolyse er en kjemisk reaksjon der man kan skille grunnstoffer fra hverandre ved hjelp av elektrisk strøm. Ved å sende strøm gjennom en elektrisk ledende løsning; en elektrolytt, vil de forskjellige grunnstoffene avsettes på hver sin elektrode, avhengig av hva slags elektrisk spenning man opererer under.
I utgangspunktet er elektrodenes formål kun å levere strøm, men noen ganger designer man prosessen sin slik at elektroden er ment å delta i reaksjonen, slik som i aluminiumsproduksjon der karbonanoder ikke bare leverer elektrisk energi, men de også leverer kjemisk energi i form av karbon som omdannes til CO2 i prosessen. En elektrode som ikke deltar i prosessen i det hele tatt, en såkalt inert anode, vil eliminere dette CO2-utslippet gjennom at den kjemiske energien fra karbon erstattes av enda mere elektrisk energi. Imidlertid er det svært utfordrende å konstruere fullstendig inerte anoder.
Siden elektrolytten må være flytende medfører dette for metallproduksjon at man enten må ha veldig høye temperaturer (for å smelte malmen), eller man bruker noen sterkt reaktive (etsende) løsninger (for å løse opp malmen), eller man bruker en kombinasjon av disse. Slike betingelser (høy temperatur, elektrisk spenning og/eller reaktiv løsning) er det svært få materialer som motstår, så elektrodene man anvender vil sakte brytes ned.
Sink, nikkel og aluminium er eksempler på viktige metaller som i dag produseres via elektrolyse.





